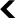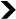Vivre sans vieillir : mythe ou réalité ?
- De nombreux investissements et travaux de recherche s’attachent à revigorer la biologie biomédicale pour mieux appréhender les mystères de la longévité.
- Contrôler les processus de vieillissement, c’est éviter toutes les maladies qui naissent par l’usure de nos organes, comme les maladies neurodégénératives.
- Il serait possible d’inverser les processus de vieillissement en reprogrammant les cellules pour les rajeunir ou en changeant la composition sanguine.
- L’Insee estime qu’en France, au moins 11 % des enfants nés après 2000 peuvent espérer devenir centenaires, voire « supercentenaires ».
- Mais, à vivre éternellement, il convient de se demander si l’Homme ne va pas mourir d’ennui ou de dépression.
Depuis quelques années, d’importantes sommes sont versées pour revigorer la recherche biomédicale et mieux comprendre le vieillissement. Ce nouvel engouement complète les efforts consentis naguère pour appréhender les mystères de la longévité. Puisque globalement la durée de vie ne cesse de croître, le défi est d’assurer une bonne santé à ces années rajoutées. Pour atteindre l’objectif, les scientifiques sont invités à repousser le mur de la longévité naturelle1 afin de vivre aisément au-delà de 115 ans2. Selon les spécialistes du vieillissement, cette quête ne serait plus une utopie comme elle le fut jadis à l’époque de Gilgamesh, ou de Faust. En revanche, en devenant réel, cet espoir soumettrait nos vies, et surtout l’équilibre de nos sociétés si sensibles à l’évolution démographique, à des bouleversements incommensurables. Voyons, sans plus tarder, les aspects scientifiques et sociétaux de cette quête de la jeunesse éternelle.
Cet article a été publié dans notre magazine Le 3,14 sur la mort. Découvrez-le ici.

Pourrons-nous vivre en bonne santé, au-delà de la centaine ?
Croissant au rythme de deux années par décennie, notre espérance de vie a déjà plus que doublé. Si elle n’était que de 27 ans pour un homme et 28 ans pour une femme en 1750, elle s’établit désormais respectivement à 80 ans et 86 ans, en France3. Pour comprendre ce phénomène spectaculaire, notons qu’il y a eu d’abord des progrès des plus significatifs sur les taux de survie des enfants dans les premières années après la naissance. Plus précisément, c’est parce que nous avons su combattre efficacement la mortalité infantile par la vaccination et les mesures d’hygiène sous la houlette des travaux de Louis Pasteur, puis un peu plus tard par l’usage des antibiotiques grâce aux découvertes d’Alexander Fleming, que l’espérance de vie moyenne s’est accrue. Plus récemment, c’est l’âge du décès qui a été la nouvelle cible des chercheurs, avec deux objectifs en tête : améliorer la qualité de vie des seniors, et réduire la charge pesant sur les systèmes de santé pour maintenir la stabilité économique et sociale de nos sociétés vieillissantes.
Contrôler les processus de vieillissement, c’est vouloir éviter toutes les maladies qui naissent par l’usure de nos organes.
Cependant, la recette est plus complexe qu’il n’y paraît. Contrôler les processus de vieillissement ou, pour être plus précis, éviter qu’ils ne menacent l’existence des individus, c’est vouloir éviter toutes les maladies qui naissent par l’usure de nos organes : maladies neurodégénératives pour le cerveau, rhumatismes pour les articulations, maladies cardiovasculaires pour le cœur, etc. Si cet objectif devait être atteint, tel le vœu de Dorian Gray, nous resterions alors d’éternels jeunes gens en attendant qu’une mort accidentelle mette un terme à notre existence. Alors, mythe ou réalité ?
Biologie du vieillissement, une science jeune
Nombre d’entreprises qui pressentent d’immenses bénéfices à venir investissent dans des laboratoires dont l’activité est centrée sur l’étude du vieillissement. Les fondateurs de Google, Larry Page et Sergey Brin, ont fait de la fontaine de jouvence leur quête ultime en créant Calico Life Sciences et Verily Life Sciences. Plus récemment, Sam Altman (de Open.AI) vient d’investir 180 millions de dollars dans une entreprise qui tente de retarder la mort, et la start-up californienne Altos Lab a réuni plus de 3 milliards de dollars en 2022 pour parvenir à inverser le vieillissement cellulaire. Cette start-up s’est même offert le luxe de recruter le prix Nobel de Médecine en 2012, le professeur Shinya Yamanaka4.
S’il est aisé de comprendre cet engouement, il est aussi facile d’en apprécier ses conséquences sur l’ensemble des acteurs de la recherche. En effet, cette nouvelle obsession détourne l’attention des travaux autrefois dédiés au traitement des maladies liées à l’âge au profit d’une meilleure compréhension des mécanismes du vieillissement. Initiée dans les années 90, cette recherche avait pour modèle d’étude des organismes simples comme un petit ver, le nématode Caenorhabditiselegans, ou la mouche à fruits (Drosophila melanogaster). En étudiant les mécanismes de survie du nématode exposé à des conditions difficiles, Gary Ruvkun découvrit l’existence d’une phase léthargique nommée « stade dauer ». Cette stase permet au nématode de survivre grâce au ralentissement de son métabolisme selon un mécanisme semblable à celui qui, chez l’Homme, contrôle la sécrétion d’insuline. À la même époque, une chercheuse en biologie moléculaire, Cynthia Kenyon, parvint à doubler l’espérance de vie du même ver en provoquant une mutation d’un gène impliqué lui aussi dans la production d’un facteur de croissance analogue à l’insuline. Il n’a pas été surprenant d’apprendre que cette chercheuse de renom fut ensuite recrutée par Calico pour en devenir sa vice-présidente. Depuis ces premiers travaux, une multitude d’études ont été développées par une communauté grandissante de scientifiques afférés à repousser la limite de la durée de vie.
Soigner le vieillissement : une révolution en sciences biologiques ?
Le vieillissement est une succession de changements responsables d’altérations qui s’amoncèlent avec l’âge, mais il doit être distingué de la maladie. Proposée initialement dans les années 2010, la biologie du vieillissement distingue une liste de caractéristiques comprenant l’instabilité du génome, le raccourcissement progressif des télomères, les altérations épigénétiques, le dysfonctionnement des mitochondries, une mauvaise régulation du repliement des protéines, la dérégulation de la détection des nutriments, la sénescence cellulaire, l’épuisement du renouvellement des cellules souches et des défauts de communication intercellulaire. Depuis, d’autres marqueurs se sont rajoutés à la liste, comme l’autophagie compromise, une dérégulation de l’épissage, un microbiome perturbé et l’inflammation plus ou moins chronique. L’addition de ces nouveaux facteurs, au moins pour les deux derniers, appuie l’idée d’une vision holiste de l’humain selon laquelle « le tout est plus que la somme de ses parties »5. Nous ne serions qu’un holobionte, c’est-à-dire une entité formée par différentes espèces qui cohabitent pour ne former qu’une seule entité écologique. Autrement dit, nous ne serions le produit, non pas seulement de nos gènes, mais d’une symbiose mutualiste entre nous (l’hôte) et nos invités (le microbiome), et le vieillissement dépendrait aussi de cet équilibre fragile.
Dans ce cas, comment se pourrait-il que le microbiome, ou son image-miroir qu’est notre système immunitaire, contribue à la biologie du vieillissement ? Nous savons que le système immunitaire reconnaît les dangers de toutes sortes, grâce à des récepteurs innés qui différencient le soi du non soi. Or, les agents microbiens, les débris cellulaires ou les nutriments interagissent avec des récepteurs qui déclenchent la réponse immunitaire innée connue pour réduire l’autophagie. Les pathologies associées au vieillissement correspondent donc à cet état chronique de dysrégulation de l’autophagie. Ceci se traduit par l’accumulation de déchets intracellulaires et d’une réaction inflammatoire chronique – un processus auto-entretenu qui aboutirait au déclin de l’organisme.
Il existe un autre axe de recherche actuellement très en vogue : rendre les processus de vieillissement réversibles. On sait aujourd’hui reprogrammer des cellules pour les rajeunir, et mon laboratoire, avec d‘autres, ont réussi à démontrer que le vieillissement cérébral pouvait être inversé en changeant la composition sanguine de sujets âgés6. Aujourd’hui, nous sommes capables de reprogrammer des processus moléculaires pour rajeunir les cellules nerveuses du cerveau7. Ces recherches prouvent déjà que des organismes comme la souris peuvent gagner plus d’un tiers de leur vie, et conserver une bonne santé mentale et physique.
Une plus longue longévité, et après ?
L’Insee estime qu’en France, au moins 11 % des enfants nés après 2000 peuvent espérer devenir centenaires, voire « supercentenaires ». Le nombre de centenaires a d’ailleurs explosé depuis les années 1960 : de 450 à l’époque, on en décompte aujourd’hui près de 30 000, dont près de 90 % sont des femmes. Les modèles des démographes prédisent qu’il pourrait y en avoir treize fois plus en 20608.
L’Insee estime qu’en France, au moins 11 % des enfants nés après 2000 peuvent espérer devenir centenaires, voire supercentenaires.
À ces estimations exagérément optimistes, il convient de rappeler que l’espérance de vie ne progresse pas de façon uniforme sur la planète. En France, elle ne progresse que très faiblement depuis quelques années quand elle recule de façon préoccupante aux États-Unis9. Depuis les années 70, les progrès en matière de prévention des maladies cardiovasculaires ont permis de sensiblement faire reculer la mortalité en réduisant ce type de maladies, mais aujourd’hui les marges de progression de cette prévention sont minimes. Leur part dans l’amélioration de l’espérance de vie devient donc négligeable.
Si les progrès scientifiques peuvent nous laisser espérer un jour de ne plus mourir de vieillesse, alors de quoi allons-nous mourir ? « Mourir de vieillesse, c’est une mort rare, singulière et extraordinaire. », écrit Michel de Montaigne dans un essai consacré à l’âge10. Comme le pensait Montaigne, nous ne connaitrions plus alors que des morts accidentelles, brutales ou bien des morts choisies. Dans ce dernier cas, la mort ne résulterait pas d’une lassitude vis-à-vis de la souffrance ou de la maladie – puisqu’elles n’existeraient plus – mais tout simplement de l’ennui, de la dépression, ou du spleen causé par la répétition inlassable et insipide des jours. Après la promesse scientifique d’une éternelle jeunesse, serions-nous condamnés au suicide assisté ?