Ce sont aux nouvelles techniques de séquençage de l’ADN que l’on peut attribuer les débuts de la médecine personnalisée. Cette approche, aussi appelée médecine de précision, cherche à individualiser chaque traitement en ciblant les mécanismes à l’origine de la maladie, en particulier du cancer.
L’analyse moléculaire des tumeurs a révélé leur incroyable diversité. Ces caractéristiques ont dessiné des sous-groupes de patients distincts, quand ils semblaient pourtant similaires du point de vue des critères cliniques. Segmenter ainsi les patients, pour que chaque sous-groupe dispose du médicament optimal, améliore la qualité des soins. « De manière ultime, on pourrait imaginer un traitement différent pour chaque patient suivant les caractéristiques moléculaires de sa tumeur », juge Alexis Gautreau, professeur de biologie à l’École polytechnique et directeur de recherche au CNRS.
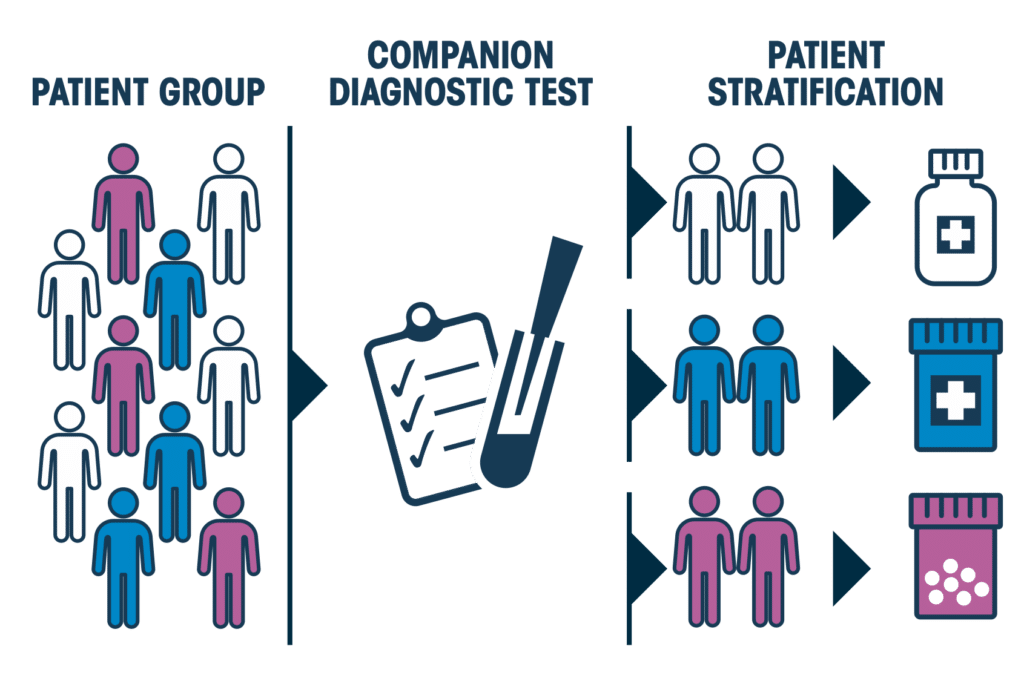
Il précise aussi la définition : « La médecine personnalisée ne concerne pas que les traitements. C’est la rencontre d’un diagnostic moléculaire et d’un médicament » ; le diagnostic donnant la recommandation pour prescrire le médicament.
Des effets spectaculaires
Les résultats obtenus ont été impressionnants, comme l’illustre le trastuzumab, un traitement contre des cancers du sein. C’est l’un des médicaments précurseurs de la médecine personnalisée. Il cible avec précision les cellules cancéreuses les plus agressives tout en épargnant les cellules saines. Désormais incontournable pour traiter les cancers du sein porteurs d’un variant génétique particulier, il a grandement amélioré la survie des patientes : par rapport à un traitement « standard » en association avec l’emtansine, il augmente la survie sans progression de plus de 3 mois et la survie globale de plus de 10 %. Désormais administré en association avec des chimiothérapies conventionnelles, il offre aux patientes plusieurs mois supplémentaires de survie.
D’autres approches visent directement la mutation. C’est notamment le cas des traitements des mélanomes cutanés (cancers de la peau) avec la mutation BRAF V600E. Ils inhibent spécifiquement la forme mutée d’une enzyme, au sein de la tumeur, sans affecter la protéine normale, dans le reste de l’organisme. Autrement dit, en corrigeant la malfonction induite par la mutation, ce traitement soigne le cancer par la racine.
Ces succès sont le fruit d’un travail conjoint de la recherche académique, des start-ups et de l’industrie. Cette dernière s’est aperçue qu’elle pouvait ressortir de ses tiroirs des molécules qu’elle avait écartées de ses développements, faute de résultats concluants. Des traitements qui avaient échoué face à une large population de malades peuvent ainsi tout de même fonctionner sur un sous-ensemble. Cette logique, dite du drug repositioning, permet d’économiser temps et argent lors du développement préclinique et des premières phases cliniques.
De plus ce n’est plus forcément la localisation du cancer qui détermine si un traitement fonctionne ou pas, mais la biologie. Un même traitement peut donc soigner à la fois des patients avec un cancer du pancréas et des patients avec un cancer du poumon.
« Les thérapies ciblées fonctionnent très bien, tout en produisant beaucoup moins d’effets secondaires que les thérapies conventionnelles, précise Alexis Gautreau. Les gens croient au miracle après ces traitements même si les rechutes sont fréquentes ».
Jusqu’à l’échappement
En effet, après plusieurs mois de régression des tumeurs, les médecins observent souvent un redémarrage de leur croissance. Le cancer « échappe » à la thérapie ciblée. L’hétérogénéité des tumeurs en est une des causes. Non seulement les altérations génétiques sont différentes si on compare les tumeurs de différents patients, mais elles varient aussi au sein d’une même tumeur, d’une cellule tumorale à l’autre.
Une thérapie ciblée fait fondre la tumeur quand elle est efficace sur la majorité des cellules. Certaines cellules meurent sous l’effet du traitement et d’autres, parce qu’elles présentent d’autres mutations, résistent. Ainsi, la thérapie ciblée ne fait souvent que sélectionner, dans la mosaïque de cellules cancéreuses, celles qui ne répondent pas au traitement. Ces dernières finissent par reformer une tumeur en lieu et place de l’originale.
La collaboration médecin-biologiste est cruciale pour aborder cette question : « Les biologistes ont beaucoup de modèles, de cultures cellulaires, de modèles de souris très astucieux. Mais ceux-ci ne représentent pas obligatoirement bien l’évolution de la maladie humaine. Une tumeur de 3 cm de diamètre chez l’homme correspond à une tumeur de 1 mm chez la souris, constituée de beaucoup moins de cellules, c’est-à-dire d’une diversité cellulaire plus faible. Soigner des souris du cancer, on sait faire ! Mais soigner des êtres humains, c’est plus compliqué », reconnaît le biologiste.
Des réponses encore cachées
Une solution logique consiste à combiner les thérapies ciblées. Mais les tumeurs s’échappent encore. Alexis Gautreau insiste : « On observe des phénomènes d’échappement que l’on ne comprend pas. Il semble que face aux médicaments, les cellules tumorales changent, accumulent des mutations qui vont leur permettre de s’en sortir ». Le phénomène est d’ailleurs plus fréquent que ne le prédisent les modélisations.
Percer ce mystère est un défi pour la recherche biomédicale, qui s’allie à l’intelligence artificielle pour le surmonter. « Si la question était crackable seulement avec des ordinateurs, ce serait super, admet Alexis Gautreau. Mais je pense qu’on a déjà assez essayé pour reconnaître qu’il nous manque à la fois des données expérimentales à mouliner et des lois de la biologie à comprendre. »








